Đề số 7 - Đề kiểm tra học kì 1 - Hóa học 11
Đề bài
I. PHẦN CHUNG CHO TẤT CẢ CÁC HỌC SINH (6 điểm)
Câu 1: (2 điểm) Viết phương trình phản ứng theo sơ đồ chuyển hóa sau: (ghi rõ điều kiện, nếu có)
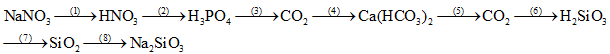
Câu 2: (2 điểm) Bằng phương pháp hóa học hãy phân biệt 4 dung dịch đựng trong các lọ mất nhãn sau: NH4Cl, Na3PO4, K2CO3, NaNO3.Viết phương trình hóa học xảy ra.
Câu 3: (2 điểm) Đốt cháy hoàn toàn 0,44g hợp chất hữu cơ A thu được 448ml khí CO2 (đktc) và 0,36g nước.
a/ Tìm công thức đơn giản nhất của A.
b/ Tìm công thức phân tử A biết tỉ khối của A so với hiđro là 44.
II. PHẦN RIÊNG (4 điểm) Học sinh học chương trình nào phải làm theo chương trình đó.
Câu 4: (2 điểm)
a/ Viết 1 phương trình hóa học chứng minh Silic có tính khử. Xác định số oxi hóa và chỉ rõ vai trò các chất tham gia phản ứng.
b/ Em hãy viết 01 phương trình điều chế cacbon monooxit (CO) bằng phương pháp khí than ướt.
Câu 5: (2 điểm) Hấp thụ hoàn toàn 3,36 lít khí CO2 (ở đktc) vào 100 ml dung dịch KOH 2M.
a/ Cho biết sau phản ứng thu được muối nào ?
b/ Tìm khối lượng muối thu được ?
Dành cho các lớp A
Câu 4: (2 điểm)
a/ Em hãy viết phương trình điều chế phân ure.
b/ Viết 01 phương trình chứng minh tính khử của Photpho, Xác định số oxi hóa và chỉ rõ vai trò các chất tham gia phản ứng.
Câu 5: (2 điểm) Dung dịch X chứa hỗn hợp gồm Na2CO3 1,5M và KHCO3 1M. Nhỏ từ từ từng giọt cho đến hết 200 ml dung dịch HCl 1M vào 100 ml dung dịch X, sinh ra V lít khí (ở đktc) và dung dịch Y. Hãy:
a/ Tìm V.
b/ Cô cạn dd Y, Tính khối lượng muối khan trong Y.
Lời giải chi tiết
I. PHẦN CHUNG CHO TẤT CẢ HỌC SINH (6 điểm)
Câu 1:
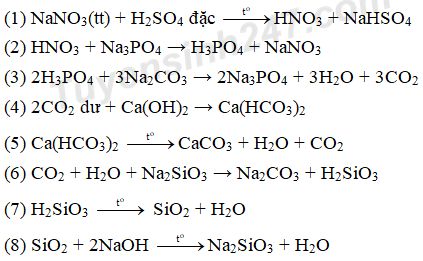
Câu 2:
| NH4Cl | Na3PO4 | K2CO3 | NaNO3 |
Dung dịch NaOH | Khí mùi khai | - | - | - |
Dung dịch HCl | x | - | Khí không màu | - |
Dung dịch AgNO3 | x | x | Kết tủa vàng | - |
NH4Cl + NaOH → NaCl + NH3↑ + H2O
K2CO3 + 2HCl → 2KCl + H2O + CO2↑
Na3PO4 + 3AgNO3 → Ag3PO4↓ + 3NaNO3
Câu 3:
nCO2 = 0,448 : 22,4 = 0,02 mol
=> nC = nCO2 = 0,02 mol => mC = 0,02.12 = 0,24 (g)
nH2O = 0,36 : 18 = 0,02 mol
=> nH = 2nH2O = 0,04 mol => mH = 0,04.1 = 0,04 (g)
mO = mA – mC – mH = 0,44 – 0,24 – 0,04 = 0,16 (g)
=> nO = 0,16 : 16 = 0,01 mol
a/ Gọi công thức phân tử của A là CxHyOz
Ta có: x : y : z = nC : nH : nO = 0,02 : 0,04 : 0,01 = 2 : 4 : 1
Vậy công thức đơn giản nhất của A là C2H4O
b/ Công thức đơn giản nhất của A là C2H4O nên công thức phân tử của A có dạng: (C2H4O)n
dA/H2 = 44 => MA = 44.2 = 88
=> 44n = 88 => n = 2
Vậy công thức phân tử của A là C4H8O2
II. PHẦN RIÊNG: (4 điểm) Học sinh học chương trình nào phải làm theo chương trình đó.
Dành cho các lớp D,T:
Câu 4:
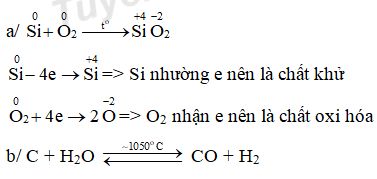
Câu 5:
a/ nCO2 = 3,36 : 22,4 = 0,15 mol, nKOH = 0,1.2 = 0,2 mol
Ta thấy: => tạo 2 muối K2CO3 và KHCO3
b/ Đặt nK2CO3 = x mol; nKHCO3 = y mol
CO2 + 2KOH → K2CO3 + H2O
x 2x x (mol)
CO2 + KOH → KHCO3
y y y (mol)
nCO2 = x + y = 0,15 (1)
nKOH = 2x + y = 0,2 (2)
Giải hệ phương trình (1) và (2):
\(\left\{ \begin{gathered}
x + y = 0,15 \hfill \\
2x + y = 0,2 \hfill \\
\end{gathered} \right. \to \left\{ \begin{gathered}
x = 0,05 \hfill \\
y = 0,1 \hfill \\
\end{gathered} \right.\)
Khối lượng của các muối thu được là:
mK2CO3 = 0,05.138 = 6,9 gam
mKHCO3 = 0,1.100 = 10 gam
Tổng khối lượng 2 muối 6,9 + 10 = 16,9 gam
Dành cho các lớp A
Câu 4:

Câu 5:
a/ nCO3 2- = 0,1.1,5 = 0,15 mol, nHCO3- = 0,1.1 = 0,1 mol, nH+ = 0,2.1 = 0,2 mol
Khi nhỏ từ từ H+ vào dung dịch hỗn hợp CO32- và HCO3- thì thứ tự phản ứng là:
H+ + CO32- → HCO3-
0,15dư 0,05 ← 0,15 → 0,15 (mol)
H+ + HCO3- → H2O + CO2
0,05 → 0,05 → 0,05 (mol)
nHCO3- sau phản ứng = 0,1 + 0,15 – 0,05 = 0,2 mol
a/ VCO2 = 0,05.22,4 = 1,12 lít
b/ Dung dịch thu được chứa:
\(\left\{ \begin{gathered}
N{a^ + }:0,3mol \hfill \\
{K^ + }:0,1mol \hfill \\
HC{O_3}^ - :0,2mol \hfill \\
C{l^ - }:0,2mol \hfill \\
\end{gathered} \right.\)
Khi cô cạn HCO3- bị phân hủy:
\(\begin{gathered}
2HC{O_3}^ - \xrightarrow{{{t^o}}}C{O_3}^{2 - } + C{O_2} + {H_2}O \hfill \\
0,2mol\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,0,1mol \hfill \\
\end{gathered} \)
Hỗn hợp muối sau khi cô cạn gồm:
\(\left\{ \begin{gathered}
N{a^ + }:0,3mol \hfill \\
{K^ + }:0,1mol \hfill \\
C{O_3}^{2 - }:0,1mol \hfill \\
C{l^ - }:0,2mol \hfill \\
\end{gathered} \right.\)
m muối = 0,3.23 + 0,1.39 + 0,1.60 + 0,2.35,5 = 23,9 gam
Xem lời giải chi tiết đề thi học kì 1 tại Xemloigiai.com
Xemloigiai.com
- Đề cương ôn tập học kỳ I môn hóa lớp 11
- Đề cương bài tập ôn tập học kì I Hóa học 11 có lời giải
- Đề số 1 - Đề kiểm tra học kì 1 - Hóa học 11
- Đề số 2 - Đề kiểm tra học kì 1 - Hóa học 11
- Đề số 3 - Đề kiểm tra học kì 1 - Hóa học 11
- Đề số 4 - Đề kiểm tra học kì 1 - Hóa học 11
- Đề số 5 - Đề kiểm tra học kì 1 - Hóa học 11
- Đề số 6 - Đề kiểm tra học kì 1 - Hóa học 11
- Đề số 8 - Đề kiểm tra học kì 1 - Hóa học 11
- Đề số 9 - Đề kiểm tra học kì 1 - Hóa học 11
- Đề số 10 - Đề kiểm tra học kì 1 - Hóa học 11
- Đề số 11 - Đề kiểm tra học kì 1 - Hóa học 11
- Đề số 12 - Đề kiểm tra học kì 1 - Hóa học 11
- Đề số 13 - Đề kiểm tra học kì 1 - Hóa học 11
- Đề số 14 - Đề kiểm tra học kì 1 - Hóa học 11
- Đề số 15 - Đề kiểm tra học kì 1 - Hóa học 11
SGK Hóa lớp 11
Giải bài tập hóa học lớp 11 đầy đủ công thức, lý thuyết, phương trình hóa học, chuyên đề hóa học SGK 11 giúp để học tốt hóa học 11, luyện thi THPT Quốc gia
CHƯƠNG 1: SỰ ĐIỆN LI
- Bài 1. Sự điện li
- Bài 2. Axit, bazơ và muối
- Bài 3. Sự điện li của nước. pH. Chất chỉ thị Axit - bazơ
- Bài 4. Phản ứng trao đổi ion trong dung dịch các chất điện li
- Bài 5. Luyện tập: Axit, bazơ và muối. Phản ứng trao đổi ion trong dung dịch các chất điện li
- Bài 6. Bài thực hành 1: Tính axit-bazơ. Phản ứng trao đổi ion trong dung dịch các chất điện li
- Đề kiểm tra 15 phút - Chương I - Hóa học 11
- Đề kiểm tra 45 phút (1 tiết) - Chương I - Hóa học 11
Đề kiểm tra giữa kì - Hóa học 11
CHƯƠNG 2: NITƠ - PHOTPHO
- Bài 7. Nitơ
- Bài 8. Amoniac và muối amoni
- Bài 9. Axit nitric và muối nitrat
- Bài 10. Photpho
- Bài 11. Axit photphoric và muối photphat
- Bài 12. Phân bón hóa học
- Bài 13. Luyện tập: Tính chất của Nitơ, photpho và các hợp chất của chúng
- Bài 14. Bài thực hành 2: Tính chất của một số hợp chất nitơ, photpho
- Đề kiểm tra 15 phút - Chương II - Hóa học 11
- Đề kiểm tra 45 phút (1 tiết) - Chương II - Hóa học 11
CHƯƠNG 3: CACBON - SILIC
- Bài 15. Cacbon
- Bài 16. Hợp chất của cacbon
- Bài 17. Silic và hợp chất của silic
- Bài 18. Công nghiệp silicat
- Bài 19. Luyện tập: Tính chất của cacbon, silic và các hợp chất của chúng
- Đề kiểm tra 15 phút - Chương III - Hóa học 11
- Đề kiểm tra 45 phút (1 tiết) - Chương III - Hóa học 11
CHƯƠNG 4: ĐẠI CƯƠNG VỀ HÓA HỌC HỮU CƠ
- Bài 20. Mở đầu về hoá học hữu cơ
- Bài 21. Công thức phân tử hợp chất hữu cơ
- Bài 22. Cấu trúc phân tử hợp chất hữu cơ
- Bài 23. Phản ứng hữu cơ
- Bài 24. Luyện tập: Hợp chất hữu cơ, công thức phân tử và công thức cấu tạo
- Đề kiểm tra 15 phút - Chương IV - Hóa học 11
- Đề kiểm tra 45 phút (1 tiết) - Chương IV - Hóa học 11
ĐỀ THI HỌC KÌ 1 MỚI NHẤT CÓ LỜI GIẢI
CHƯƠNG 5: HIDROCACBON NO
- Bài 25. Ankan
- Bài 26. Xicloankan
- Bài 27. Luyện tập ankan và xicloankan
- Bài 28. Bài thực hành số 3 : Phân tích định tính nguyên tố. Điều chế và tính chất của metan
- Đề kiểm tra 15 phút - Chương V - Hóa học 11
- Đề kiểm tra 45 phút (1 tiết) - Chương V - Hóa học 11
CHƯƠNG 6: HIDROCACBON KHÔNG NO
- Bài 29. Anken
- Bài 30. Ankađien
- Bài 31. Luyện tập: Anken và Ankadien
- Bài 32. Ankin
- Bài 33. Luyện tập: Ankin
- Bài 34. Bài thực hành 4 : Điều chế và tính chất của etilen và axetilen
- Đề kiểm tra 15 phút - Chương VI - Hóa học 11
- Đề kiểm tra 45 phút (1 tiết) - Chương VI - Hóa học 11
CHƯƠNG 7: HIĐROCACBON THƠM, NGUỒN HIĐROCACBON THIÊN NHIÊN. HỆ THỐNG HÓA VỀ HIĐROCACBON
- Bài 35. Benzen và đồng đẳng. Một số hiđrocacbon thơm khác
- Bài 36. Luyện tập: Hiđrocacbon thơm
- Bài 37. Nguồn Hiđrocacbon thiên nhiên
- Bài 38. Hệ thống hóa về hiđrocacbon
- Đề kiểm tra 15 phút - Chương VII - Hóa học 11
- Đề kiểm tra 45 phút (1 tiết) - Chương VII - Hóa học 11
CHƯƠNG 8: DẪN XUẤT HALOGEN - ANCOL - PHENOL
- Bài 39. Dẫn xuất halogen của hiđrocacbon
- Bài 40. Ancol
- Bài 41. Phenol
- Bài 42. Luyện tập: Dẫn xuất halogen, ancol và phenol
- Bài 43. Bài thực hành 5: Tính chất của etanol, glixerol và phenol
- Đề kiểm tra 15 phút - Chương VIII - Hóa học 11
- Đề kiểm tra 45 phút (1 tiết) - Chương VIII - Hóa học 11
CHƯƠNG 9: ANĐEHIT - XETON - AXIT CACBOXYLIC
- Bài 44. Anđehit - xeton
- Bài 45. Axit cacboxylic
- Bài 46. Luyện tập: Anđehit - xeton - axit cacboxylic
- Bài 47. Bài thực hành 6: Tính chất của anđehit và axit cacboxylic
- Đề kiểm tra 15 phút - Chương IX - Hóa học 11
- Đề kiểm tra 45 phút (1 tiết) - Chương IX - Hóa học 11
Xem Thêm
Lớp 11 | Các môn học Lớp 11 | Giải bài tập, đề kiểm tra, đề thi Lớp 11 chọn lọc
Danh sách các môn học Lớp 11 được biên soạn theo sách giáo khoa mới của bộ giáo dục đào tạo. Kèm theo lời giải sách bài tập, sách giáo khoa, đề kiểm tra 15 phút, 45 phút (1 tiết), đề thi học kì 1 và học kì 2 năm học 2024 ngắn gọn, chi tiết dễ hiểu.
Toán Học
Vật Lý
Hóa Học
Ngữ Văn
- Soạn văn 11
- SBT Ngữ văn lớp 11
- Văn mẫu 11
- Soạn văn 11 chi tiết
- Soạn văn ngắn gọn lớp 11
- Soạn văn 11 siêu ngắn
Sinh Học
GDCD
Tin Học
Tiếng Anh
Công Nghệ
Lịch Sử & Địa Lý
- Tập bản đồ Địa lí lớp 11
- SBT Địa lí lớp 11
- SGK Địa lí lớp 11
- Tập bản đồ Lịch sử lớp 11
- SBT Lịch sử lớp 11
- SGK Lịch sử lớp 11