Đề kiểm tra 45 phút (1 tiết) – Đề số 3 – Chương 4 – Hóa học 9
Đề bài
I.Trắc nghiệm khách quan (4 điểm: mỗi câu 0,5 điểm)
Câu 1: Để phân biệt các khí CH4 và H2 người ta
A.đốt từng khí, khí nào cháy được trong khí Cl2 là CH4.
D.đốt từng khí trong bình đựng O2 sau đó rót dung dịch Ca(OH)2 vào bình rồi lắc nhẹ, bình có kết tủa trắng thì khí ban đầu là CH4.
C.chỉ cần biết khí không tan trong nước là khí CH4.
D.chỉ cần biết chất vô cơ là H2.
Câu 2: Cấu tạo phân tử etilen và axetilen khác nhau do
A.số nguyên tử C trong mỗi phân tử.
B.tính chất của chúng khác nhau.
C.etilen có liên kết đôi còn axetilen có liên kết ba.
D.C trong etilen có hóa trị II, còn C trong axetilen có hóa trị I.
Câu 3: Một hữu chất cơ Z khi đốt phản ứng xảy ra theo phương trình:
aZ + 2O2 \(\to\) CO2 + 2H2O.
Công thức phân tử của Z là (a là số nguyên dương)
A.C2H4 B.C3H6
C.C3H8 D.CH4.
Câu 4: Cho phương trình: C6H6 + Br2 \(\to\) C6H5Br + HBr (Fe)
Trong đó:
A.C6H6 là chất lỏng, Br2 là chất khí.
B.C6H5Br là chất lỏng không màu.
C.HBr là chất khí màu nâu đỏ.
D.phản ứng xảy ra ở nhiệt độ rất thấp.
Câu 5: Một bình kín chứa hỗn hợp khí C2H4 và O2, trong bình có mặt dung dịch Br2. Đốt cháy hỗn hợp bằng tia lửa điện, lắc nhẹ bình người ta thấy
A.màu nâu dung dịch Br2 nhạt một phần chứng tỏ C2H4 còn.
B.khối lượng bình nặng hơn so với trước khi đốt.
C.nhiệt độ trong bình không đổi.
D.khối lượng dung dịch Br2 giảm.
Câu 6: Một hidrocacbon X mạch hở, có một liên kết ba trong phân tử. Khi cho 5,2 gam X tác dụng hết với 400ml dung dịch Br2 1M.
X có công thức cấu tạo thu gọn là (H = 1, C = 12)
\(\eqalign{ & A.C{H_3} - CH = C{H_2} \cr & B.C{H_3} - C \equiv CH \cr & C.HC \equiv CH. \cr & D.C{H_3} - C{H_3}. \cr} \)
Câu 7: Cho quá trình: dầu nặng -> xăng + hỗn hợp khí. Quá trình này có tên gọi là:
A.sự phân hủy
B.quá trình crackinh.
C.quá trình trùng hợp.
D.sự chưng cất dầu mỏ.
Câu 8: Một hỗn hợp gồm etilen và metan khi cho qua dung dịch brom dư thì dung dịch tăng 5,6 gam đồng thời có 5,6 lít chất khí bay ra (đktc).
Thành phần % theo thể tích của etilen ban đầu là (H = 1, C = 20)
A.55,56% B.45,45%
C.33,33% D.44,44%.
II.Tự luận (6 điểm)
Câu 9 (2 điểm): Mạch cacbon là gì? Có bao nhiêu loại mạch cacbon?
Mỗi loại mạch cacbon lấy 1 ví dụ.
Câu 10 (2 điểm): Butan là một hidrocacbon có tính chất tương tự metan và có công thức phân tử là C4H10.
a)Viết công thức cấu tạo của butan.
b)Viết phương trình phản ứng đốt cháy butan.
c)Viết phương trình phản ứng thế với clo.
Câu 11 ( 2 điểm): Đốt cháy hoàn toàn 3,2 gam chất hữu cơ A sản phẩm CO2, và hơi H2O, tạo ra cho qua bình (1) đựng H2SO4 đặc, rồi qua bình (2) đựng dung dịch Ca(OH)2 (dư).
Độ tăng khối lượng (1) là 7,2 gam, bình (2) thu được 20 gam kết tủa.
a)Xác định thành phần % theo khối lượng các nguyên tố trong A.
b) Lập công thức phân tử chất A, biết tỉ khối hơi của A so với không khí là 0,5517. (Cho H = 1, C = 12, O = 16, Ca = 40, Mkk = 29)
Lời giải chi tiết
1.Đáp án
Câu | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
Đáp án | B | D | D | B | A | C | B | D |
2.Lời giải
I.Trắc nghiệm khách quan (4 điểm: mỗi câu 0,5 điểm)
Câu 1: (B)
\(\eqalign{ & C{H_4} + 2{O_2} \to C{O_2} + 2{H_2}O \cr & C{O_2} + Ca{(OH)_2} \to CaC{O_3} \downarrow + {H_2}O \cr} \)
Câu 2: (D)
Công thức cấu tạo của etilen và axetilen: \(C{H_2} = {\rm{ }}C{H_2},CH \equiv CH.\)
Câu 3: (D)
Bảo toàn nguyên tố ở 2 vế của phương trình a = 1 \(\Rightarrow \) Z là CH4
Câu 4: (B)
Phương trình: \({C_6}{H_6}(l) + B{r_2}(l) \to {C_6}{H_5}Br(l) + HBr(kkm)\)
Câu 5: (A)
Phương trình phản ứng đốt cháy C2H4:
C2H4 + 3O2 \(\to\) 2CO2 + 2H2O
-Khi đốt với tỉ lệ thể tích O2 ít hơn 3 lần thể tích C2H4 thì C2H4 còn
Sau đó tác dụng với dung dịch brom làm màu nâu dung dịch Br2 nhạt dần.
C2H4 + Br2 \(\to\) C2H4Br2
-Khối lượng bình không đổi.
- Nhiệt độ trong bình tăng do phản ứng tỏa nhiệt
- Khối lượng dung dịch brom không giảm đi.
Câu 6: (C)
Công thức chung của một hdrcacbon mạch hở, có một liên kết ba là CnH2n-2.
\(\eqalign{ & {C_n}{H_{2n - 2}} + 2B{r_2} \to {C_n}{H_{2n - 2}}B{r_4} \cr & {n_X} = {{0,4} \over 2} = 0,2mol \cr&\Rightarrow M = {{5,2} \over {0,2}} = 26 \cr} \)
Công thức phân tử của X: C2H2
Công thức cấu tạo thu gọn của X là: \(HC \equiv CH\)
Câu 7: (B)
Câu 8: (D)
Hỗn hợp etilen và metan khi cho qua dung dịch brom chỉ có etilen tác dụng theo phương trình:
C2H4 + Br2 \(\to\) C2H4Br2
Khí bay ra là metan có thể tích 5,6 lít.
Khối lượng etilen = 5,6 gam hay \(\eqalign{ & {{5,6} \over {22,4}} = 0,2mol. \cr & {V_{{C_2}{H_4}}} = 0,2.22,4 = 4,48lit(dktc) \cr} \)
Vậy thành phần % theo thể tích của etilen là: \({{4,48} \over {4,48 + 5,6}}.100\% = 44,44\% \)
II.Tự luận (6 điểm)
Câu 9:
Mạch cacbon: Những nguyên tử cacbon trong phân tử chất hữu cơ có thể liên kết trực tiếp với nhau tạo thành mạch cacbon.
Ví dụ: Mạch thẳng: CH3 – CH2 – CH2 – CH3
-Mạch nhánh: 
-Mạch vòng: 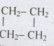
Câu 10:
a)Công thức cấu tạo của butan: CH3 – CH2 – CH2 – CH3
b)Phương trình phản ứng đốt cháy butan:
\({C_4}{H_{10}} + {{13} \over 2}{O_2} \to 4C{O_2} + 5{H_2}O\)
c)Phương trình phản ứng thế với clo:
C4H10 + Cl2 \(\to\) C4H9Cl + HCl
Câu 11:
a)Thành phần % khối lượng các nguyên tố:
Độ tăng khối lượng bình (1) bằng khối lượng H2O = 7,2 gam
\(\eqalign{ & \Rightarrow {m_H} = {{7,2} \over 9} = 0,8gam \cr & \% {m_H} = {{0,8} \over {3,2}}.100\% = 25\% \cr & C{O_2} + Ca{(OH)_2} \to CaC{O_3} \downarrow + {H_2}O \cr & {n_{C{O_2}}} = {n_{CaC{O_3}}} = {2 \over {100}} = 0,2mol \cr & \Rightarrow {m_C} = {{0,2} \over {12}} = 2,4gam \cr & \% {m_C} = {{2,4} \over {3,2}}.100\% = 75\% \cr} \)
b)Công thức phân tử: Chất A chỉ có 2 nguyên tố C, H
nC : nH = 0,2:0,8 = 1:4
\( \Rightarrow \) Công thức đơn giản nhất: CH4
Mặt khác khối lượng phân tử \(= 0,5517.29 = 16\)
\(M = (12+ 4)n = 16 \Rightarrow n = 1\)
Vậy công thức phân tử của A: CH4
Xemloigiai.com
- Đề kiểm tra 45 phút (1 tiết) – Đề số 1 – Chương 4 – Hóa học 9
- Đề kiểm tra 45 phút (1 tiết) – Đề số 2 – Chương 4 – Hóa học 9
- Đề kiểm tra 45 phút (1 tiết) – Đề số 4 – Chương 4 – Hóa học 9
SGK Hóa lớp 9
Giải bài tập hóa học lớp 9 đầy đủ công thức, lý thuyết, phương trình hóa học, chuyên đề hóa học SGK 9 giúp để học tốt hóa học 9
CHƯƠNG 1: CÁC LOẠI HỢP CHẤT VÔ CƠ
- Bài 1. Tính chất hóa học của oxit. Khái quát về sự phân loại oxit
- Bài 2. Một số oxit quan trọng
- Bài 3. Tính chất hóa học của axit
- Bài 4. Một số axit quan trọng
- Bài 5. Luyện tập: Tính chất hóa học của oxit và axit
- Bài 6. Thực hành: Tính chất hóa học của oxit và axit
- Bài 7. Tính chất hóa học của bazơ
- Bài 8. Một số bazơ quan trọng
- Bài 9. Tính chất hóa học của muối
- Bài 10. Một số muối quan trọng
- Bài 11. Phân bón hóa học
- Bài 12. Mối quan hệ giữa các loại chất vô cơ
- Bài 13. Luyện tập chương 1: Các hợp chất vô cơ
- Bài 14. Thực hành: Tính chất hóa học của bazơ và muối
- Đề kiểm tra 15 phút - Chương 1 - Hóa học 9
- Đề kiểm tra 45 phút (1 tiết) - Chương 1 - Hóa học 9
Đề thi giữa học kì - Hóa học 9
CHƯƠNG 2: KIM LOẠI
- Bài 15. Tính chất vật lí của kim loại
- Bài 16. Tính chất hoá học của kim loại
- Bài 17. Dãy hoạt động hoá học của kim loại
- Bài 18. Nhôm
- Bài 19. Sắt
- Bài 20. Hợp kim sắt: Gang, thép
- Bài 21. Sự ăn mòn kim loại và bảo vệ kim loại không bị ăn mòn
- Bài 22. Luyện tập chương 2: Kim loại
- Bài 23. Thực hành: Tính chất hóa học của nhôm và sắt
- Bài 24. Ôn tập học kì 1
- Đề kiểm tra 15 phút - Chương 2 - Hóa học 9
- Đề kiểm tra 45 phút (1 tiết) - Chương 2 - Hóa học 9
Đề thi học kì 1 mới nhất có lời giải
CHƯƠNG 3: SƠ LƯỢC VỀ BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
- Bài 25. Tính chất của phi kim
- Bài 26. Clo
- Bài 27. Cacbon
- Bài 28. Các oxit của cacbon
- Bài 29. Axit cacbonic và muối cacbonat
- Bài 30. Silic. Công nghiệp silicat.
- Bài 31. Sơ lược về bảng tuần hoàn các nguyên tố hoá học
- Bài 32. Luyện tập chương 3: Phi kim - Sơ lược về bảng tuần hoàn các nguyên tố hoá học
- Bài 33. Thực hành: Tính chất hóa học của phi kim và hợp chất của chúng
- Đề kiểm tra 15 phút - Chương 3 – Hóa học 9
CHƯƠNG 4: HIĐROCACBON. NHIÊN LIỆU
- Bài 34. Khái niệm về hợp chất hữu cơ và hoá học hữu cơ
- Bài 35. Cấu tạo phân tử hợp chất hữu cơ
- Bài 36. Metan
- Bài 37. Etilen
- Bài 38. Axetilen
- Bài 39. Benzen
- Bài 40. Dầu mỏ và khí thiên nhiên
- Bài 41. Nhiên liệu
- Bài 42. Luyện tập chương 4: Hiđrocacbon. Nhiên liệu
- Bài 43. Thực hành: Tính chất của Hiđrocacbon
- Đề kiểm tra 15 phút - Chương 4 - Hóa học 9
- Đề kiểm tra 45 phút (1 tiết) - Chương 4 - Hóa học 9
CHƯƠNG 5: DẪN XUẤT CỦA HIĐROCACBON. POLIME
- Bài 44. Rượu etylic
- Bài 45. Axit axetic
- Bài 46. Mối liên hệ giữa etilen, rượu etylic và axit axetic
- Bài 47. Chất béo
- Bài 48. Luyện tập rượu etylic, axit axetic và chất béo
- Bài 49. Thực hành: Tính chất của rượu và axit
- Bài 50. Glucozơ
- Bài 51. Saccarozơ
- Bài 52. Tinh bột và xenlulozơ
- Bài 53. Protein
- Bài 54. Polime
- Bài 55. Thực hành: Tính chất của gluxit
- Bài 56. Ôn tập cuối năm - Hóa học 9
- Đề kiểm tra 15 phút - Chương 5 - Hóa học 9
- Đề kiểm tra 45 phút (1 tiết) - Chương 5 - Hóa học 9
Xem Thêm
Lớp 9 | Các môn học Lớp 9 | Giải bài tập, đề kiểm tra, đề thi Lớp 9 chọn lọc
Danh sách các môn học Lớp 9 được biên soạn theo sách giáo khoa mới của bộ giáo dục đào tạo. Kèm theo lời giải sách bài tập, sách giáo khoa, đề kiểm tra 15 phút, 45 phút (1 tiết), đề thi học kì 1 và học kì 2 năm học 2025 ngắn gọn, chi tiết dễ hiểu.
Toán Học
Vật Lý
Hóa Học
Ngữ Văn
- SBT Ngữ văn lớp 9
- Đề thi vào 10 môn Văn
- Tác giả - Tác phẩm văn 9
- Văn mẫu lớp 9
- Vở bài tập Ngữ văn lớp 9
- Soạn văn 9 chi tiết
- Soạn văn 9 ngắn gọn
- Soạn văn 9 siêu ngắn
Sinh Học
GDCD
Tin Học
Tiếng Anh
- SBT Tiếng Anh lớp 9
- Đề thi vào 10 môn Anh
- SGK Tiếng Anh lớp 9
- SBT Tiếng Anh lớp 9 mới
- Vở bài tập Tiếng Anh 9
- SGK Tiếng Anh lớp 9 Mới
Công Nghệ
Lịch Sử & Địa Lý
- Tập bản đồ Địa lí lớp 9
- SBT Địa lí lớp 9
- VBT Địa lí lớp 9
- SGK Địa lí lớp 9
- Tập bản đồ Lịch sử lớp 9
- SBT Lịch sử lớp 9
- VBT Lịch sử lớp 9
- SGK Lịch sử lớp 9