Đề kiểm tra 1 tiết (45 phút) - Đề số 4 - Chương II - Hóa học 11
Đề bài
I. PHẦN TRẮC NGHIỆM
Câu 1. Nén hỗn hợp gồm 4 lít khí nitơ và 14 lít khí hiđro (ở cùng điều kiện nhiệt độ và áp suất) trong bình phản ứng ở nhiệt độ và xúc tac thích hợp. Sau phản ứng, đưa bình về nhiệt độ ban đầu thu đưọc 16,4 lít hỗn hợp khí. Thể tích khí amoniac thu được là:
A.2,00 lít B.1,75 lít
C.1,60 lít D.2,25 lít
Câu 2. Dẫn 4 lít khí NO và 4 lít O2, sau phản ứng xảy ra hoàn toàn, thể tích khí thu được là bao nhiêu? Biết các khí đo ở cùng điều kiện nhiệt độ và áp suất.
A.3 lít B.4 lít
C.5 lít D. 6 lít
Câu 3. Amoniac phản ứng được với nhóm các chất nào sau đây?
\(\begin{array}{l}A.C{l_2},CuO,Ca{\left( {OH} \right)_2},HN{O_3},{\rm{dd FeC}}{{\rm{l}}_2}\\B.C{l_2},HN{O_3},CuO,{O_2},{\rm{dd FeC}}{{\rm{l}}_3}\\C.C{l_2},HN{O_3},KOH,{O_2},CuO\\D.CuO,Fe{\left( {OH} \right)_3},{O_2},C{l_2}\end{array}\)
Câu 4. Khi dẫn khí NH3 vào bình chứa Cl2 thì phản ứng tạo ra “khói” trắng. Hợp chất tạo thành có công thức hóa học là:
A. N2 B. NH3
C. NH4Cl D.HCl
Câu 5. Dung dịch amoniac có thể hòa tan được Zn(OH)2 là do nguyên nhân nào sau đây?
A. Do Zn(OH)2 là một bazơ ít tan
B. Do Zn(OH)2 có khả năng tạo thành phức chất tan
C. Do Zn(OH)2 là một bazơ lưỡng tính
D. Do NH3 là một hợp chất có cực và là một bazơ yếu
Câu 6. Có thể phân biệt muối amoni với các muối khác bằng cách nào cho nó tác dụng với kiềm mạnh, vì lí do nào sau đây?
A. Muối amoni sẽ chuyển hóa thành màu đỏ
B. Có giải phóng một chất khí không màu có mùi khai
C. Có giải phóng một chất khí màu nâu đỏ
D. Giải phóng một chất không màu, không mùi
Câu 7. Hòa tan hoàn toàn 11,2 gam bột sắt vào dung dịch HNO3 đặc, nóng, dư thu được V lít khí NO2 (đktc). Giá trị của V là:
A. 4,48 lít B. 14,40 lít
C. 13,44 lít D. 6,72 lít
Câu 8. Khi cân bằng: \({N_2} + 3{H_2} \to 2N{H_3}\) được thiết lập, nồng độ cácchất như sau: \(\left[ {{N_2}} \right] = 3M;\left[ {{H_2}} \right] = 9M;\left[ {N{H_3}} \right] = 1M.\) Nồng độ ban đầu của N2 là:
A.3,9M B.3,7M
C.3,6M D.3,5M
II. PHẦN TỰ LUẬN
Câu 9. Cho 11 gam hỗn hợp Al và Fe vào dung dịch HNO3 loãng dư, thu được 6,72 lít (đktc) NO bay ra. Tính phần trăm theo khôi lượng mỗi kim loại trong hỗn hợp ban đầu?
Câu 10. Để trung hòa hoàn toàn dung dịch thu được khi thủy phân 4,54 gam một photpho trihalogenua cần 55 ml dung dịch NaOH 3M. Xác định công thức photpho trihalogenua đem dùng ở trên?
Câu 11. Hòa tan hết x gam bột nhôm vào dung dịch HNO3 đặc, nóng thu được hỗn hợp khí gồm 1,008 lít N2O và 3,36 lít NO2 (các khí đo ở đktc ). Xác định giá trị của x.
Lời giải chi tiết
I. PHẦN TRẮC NGHIỆM
Câu | 1 | 2 | 3 | 4 |
Đáp án | C | D | B | C |
Câu | 5 | 6 | 7 | 8 |
Đáp án | B | B | C | D |
Câu 1:
Ta có phương trình:
N2 + 3H2 ó 2NH3
Ban đầu 4 14
Phản ứng x 3x 2x
Sau pu 4-x 14-3x 2x
=> 4 –x + 14 – 3x + 2x = 16,4
=> 18 – 2x = 16,4
=> 2x = 1,6 lít
=> Thể tích NH3 thu được là 1,6 lít
Đáp án C
Câu 2:
Ta có phương trình:
NO + ½ O2 → NO2
Ban đầu 4 4
P ứ 4 2 4
Sau p ứ 0 2 4
=> Khi sau phản ứng thu được có thể tích là: 4+ 2 = 6 lít
Đáp án D
Câu 3:
Đáp án B
Câu 4:
NH3 + Cl2 → N2 + HCl
NH3 + HCl → NH4Cl
Đáp án C
Câu 5:
NH3 + Zn(OH)2 → [Zn(NH3)4](OH)2
Đáp án B
Câu 6:
Đáp án B
Câu 7:
n Fe = 11, 2 : 56 = 0,2 mol
Áp dụng định luật bảo toàn electron
Tổng e nhường bằng tổng e nhận
=> 3 . n Fe = n NO2
=> 3 . 0,2 = n NO2
=> n NO2 = 0,6 mol
V NO2 = 0,6 . 22,4 = 13,44 lít
Đáp án C
Câu 8:
Gọi nồng độ ban đầu của N2 là x
Ta có phương trình hóa học:
N2 + 3H2 ó 2NH3
Ban đầu x y
Phản ứng 0,5 1,5 1
Sau pu x-0,5 y – 1,5 1
=> x – 0,5 = 3 => x = 3,5M
Đáp án D
II. PHẦN TỰ LUẬN
Câu 9.
Ta có: \({n_{NO}} = \dfrac{{6,72}}{{22,4}} = 0,3\left( {mol} \right)\)
Cách 1.
Gọi a là số mol của Al và b là số mol của Fe
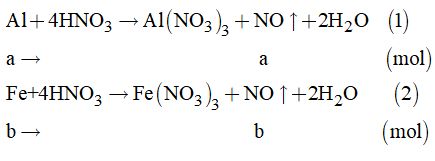
Theo đề bài, ta có hệ phương trình: \(\left\{ \begin{array}{l}27a + 56b = 11\\a + b = \dfrac{{6,72}}{{22,4}}\end{array} \right. = 0,3\)
Giải hệ phương trình ta có: \(\left\{ \begin{array}{l}a = 0,2\\b = 0,1\end{array} \right.\)
Vậy: \(\begin{array}{l}\% {m_{Al}} = \dfrac{{0,2 \times 27}}{{11}} \times 100\% = 49,1\% \\\% {m_{Fe}} = 100\% - 49,1\% = 50,9\% \end{array}\)
Cách 2.
Gọi a là khối lượng của Al \( \Rightarrow {n_{Al}} = \dfrac{a}{{27}}\left( {mol} \right)\)
Và khối lượng của Fe là: \(\left( {11 - a} \right)gam \Rightarrow {n_{Fe}} = \dfrac{{11 - a}}{{56}}\left( {mol} \right)\)
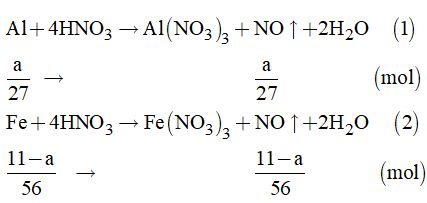
Theo đề bài, ta có phương trình:
\(\begin{array}{l}\sum {{n_{NO}}} = \dfrac{a}{{27}} + \dfrac{{11 - a}}{{56}} = 0,3\\ \Leftrightarrow 56a + 297 - 27a = 453,6\\ \Leftrightarrow 29a = 156,6 \Rightarrow a = 5,4\end{array}\)
Vậy: \(\begin{array}{l}\% {m_{Al}} = \dfrac{{5,4}}{{11}} \times 100\% = 49,1\% \\\% {m_{Fe}} = 100\% - 49,1\% = 50,9\% \end{array}\)
Câu 10.
Ta có: \({n_{NaOH}} = 0,055 \times 3 = 0,165\left( {mol} \right)\)
Gọi X là halogen trong hợp chất.
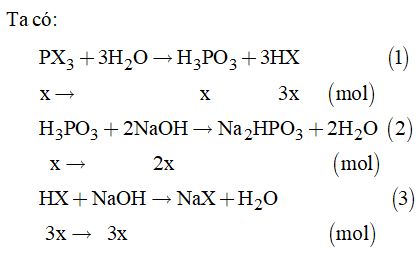
Từ (2) và (3) \( \Rightarrow 5x = 0,165 \Rightarrow x = 0,033\left( {mol} \right)\)
Mà \({n_{P{X_3}}} = \dfrac{{4,54}}{{31 + 3X}} = 0,033 \)
\(\Rightarrow X = 35,5:clo\left( {Cl} \right)\)
Câu 11.
Ta có: \({n_{{N_2}O}} = \dfrac{{1,008}}{{22,4}} = 0,045\left( {mol} \right);\)
\({n_{N{O_2}}} = \dfrac{{3,36}}{{22,4}} = 0,15\left( {mol} \right)\)
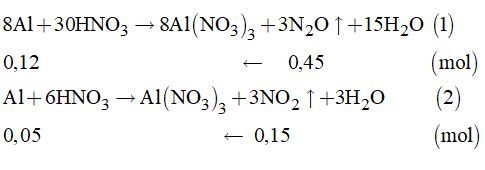
Từ (1) và (2) \( \Rightarrow \sum {{n_{Al}}} = 0,12 + 0,05 = 0,17\left( {mol} \right)\)
Vậy: \({m_{Al}} = 0,17 \times 27 = 4,59\left( {gam} \right)\).
Xemloigiai.com
- Đề kiểm tra 1 tiết (45 phút) - Đề số 1 - Chương II - Hóa học 11
- Đề kiểm tra 1 tiết (45 phút) - Đề số 2 - Chương II - Hóa học 11
- Đề kiểm tra 1 tiết (45 phút) - Đề số 3 - Chương II - Hóa học 11
- Đề kiểm tra 1 tiết (45 phút) - Đề số 5 - Chương II - Hóa học 11
SGK Hóa lớp 11
Giải bài tập hóa học lớp 11 đầy đủ công thức, lý thuyết, phương trình hóa học, chuyên đề hóa học SGK 11 giúp để học tốt hóa học 11, luyện thi THPT Quốc gia
CHƯƠNG 1: SỰ ĐIỆN LI
- Bài 1. Sự điện li
- Bài 2. Axit, bazơ và muối
- Bài 3. Sự điện li của nước. pH. Chất chỉ thị Axit - bazơ
- Bài 4. Phản ứng trao đổi ion trong dung dịch các chất điện li
- Bài 5. Luyện tập: Axit, bazơ và muối. Phản ứng trao đổi ion trong dung dịch các chất điện li
- Bài 6. Bài thực hành 1: Tính axit-bazơ. Phản ứng trao đổi ion trong dung dịch các chất điện li
- Đề kiểm tra 15 phút - Chương I - Hóa học 11
- Đề kiểm tra 45 phút (1 tiết) - Chương I - Hóa học 11
Đề kiểm tra giữa kì - Hóa học 11
CHƯƠNG 2: NITƠ - PHOTPHO
- Bài 7. Nitơ
- Bài 8. Amoniac và muối amoni
- Bài 9. Axit nitric và muối nitrat
- Bài 10. Photpho
- Bài 11. Axit photphoric và muối photphat
- Bài 12. Phân bón hóa học
- Bài 13. Luyện tập: Tính chất của Nitơ, photpho và các hợp chất của chúng
- Bài 14. Bài thực hành 2: Tính chất của một số hợp chất nitơ, photpho
- Đề kiểm tra 15 phút - Chương II - Hóa học 11
- Đề kiểm tra 45 phút (1 tiết) - Chương II - Hóa học 11
CHƯƠNG 3: CACBON - SILIC
- Bài 15. Cacbon
- Bài 16. Hợp chất của cacbon
- Bài 17. Silic và hợp chất của silic
- Bài 18. Công nghiệp silicat
- Bài 19. Luyện tập: Tính chất của cacbon, silic và các hợp chất của chúng
- Đề kiểm tra 15 phút - Chương III - Hóa học 11
- Đề kiểm tra 45 phút (1 tiết) - Chương III - Hóa học 11
CHƯƠNG 4: ĐẠI CƯƠNG VỀ HÓA HỌC HỮU CƠ
- Bài 20. Mở đầu về hoá học hữu cơ
- Bài 21. Công thức phân tử hợp chất hữu cơ
- Bài 22. Cấu trúc phân tử hợp chất hữu cơ
- Bài 23. Phản ứng hữu cơ
- Bài 24. Luyện tập: Hợp chất hữu cơ, công thức phân tử và công thức cấu tạo
- Đề kiểm tra 15 phút - Chương IV - Hóa học 11
- Đề kiểm tra 45 phút (1 tiết) - Chương IV - Hóa học 11
ĐỀ THI HỌC KÌ 1 MỚI NHẤT CÓ LỜI GIẢI
CHƯƠNG 5: HIDROCACBON NO
- Bài 25. Ankan
- Bài 26. Xicloankan
- Bài 27. Luyện tập ankan và xicloankan
- Bài 28. Bài thực hành số 3 : Phân tích định tính nguyên tố. Điều chế và tính chất của metan
- Đề kiểm tra 15 phút - Chương V - Hóa học 11
- Đề kiểm tra 45 phút (1 tiết) - Chương V - Hóa học 11
CHƯƠNG 6: HIDROCACBON KHÔNG NO
- Bài 29. Anken
- Bài 30. Ankađien
- Bài 31. Luyện tập: Anken và Ankadien
- Bài 32. Ankin
- Bài 33. Luyện tập: Ankin
- Bài 34. Bài thực hành 4 : Điều chế và tính chất của etilen và axetilen
- Đề kiểm tra 15 phút - Chương VI - Hóa học 11
- Đề kiểm tra 45 phút (1 tiết) - Chương VI - Hóa học 11
CHƯƠNG 7: HIĐROCACBON THƠM, NGUỒN HIĐROCACBON THIÊN NHIÊN. HỆ THỐNG HÓA VỀ HIĐROCACBON
- Bài 35. Benzen và đồng đẳng. Một số hiđrocacbon thơm khác
- Bài 36. Luyện tập: Hiđrocacbon thơm
- Bài 37. Nguồn Hiđrocacbon thiên nhiên
- Bài 38. Hệ thống hóa về hiđrocacbon
- Đề kiểm tra 15 phút - Chương VII - Hóa học 11
- Đề kiểm tra 45 phút (1 tiết) - Chương VII - Hóa học 11
CHƯƠNG 8: DẪN XUẤT HALOGEN - ANCOL - PHENOL
- Bài 39. Dẫn xuất halogen của hiđrocacbon
- Bài 40. Ancol
- Bài 41. Phenol
- Bài 42. Luyện tập: Dẫn xuất halogen, ancol và phenol
- Bài 43. Bài thực hành 5: Tính chất của etanol, glixerol và phenol
- Đề kiểm tra 15 phút - Chương VIII - Hóa học 11
- Đề kiểm tra 45 phút (1 tiết) - Chương VIII - Hóa học 11
CHƯƠNG 9: ANĐEHIT - XETON - AXIT CACBOXYLIC
- Bài 44. Anđehit - xeton
- Bài 45. Axit cacboxylic
- Bài 46. Luyện tập: Anđehit - xeton - axit cacboxylic
- Bài 47. Bài thực hành 6: Tính chất của anđehit và axit cacboxylic
- Đề kiểm tra 15 phút - Chương IX - Hóa học 11
- Đề kiểm tra 45 phút (1 tiết) - Chương IX - Hóa học 11
Xem Thêm
Lớp 11 | Các môn học Lớp 11 | Giải bài tập, đề kiểm tra, đề thi Lớp 11 chọn lọc
Danh sách các môn học Lớp 11 được biên soạn theo sách giáo khoa mới của bộ giáo dục đào tạo. Kèm theo lời giải sách bài tập, sách giáo khoa, đề kiểm tra 15 phút, 45 phút (1 tiết), đề thi học kì 1 và học kì 2 năm học 2025 ngắn gọn, chi tiết dễ hiểu.
Toán Học
Vật Lý
Hóa Học
Ngữ Văn
- Soạn văn 11
- SBT Ngữ văn lớp 11
- Văn mẫu 11
- Soạn văn 11 chi tiết
- Soạn văn ngắn gọn lớp 11
- Soạn văn 11 siêu ngắn
Sinh Học
GDCD
Tin Học
Tiếng Anh
Công Nghệ
Lịch Sử & Địa Lý
- Tập bản đồ Địa lí lớp 11
- SBT Địa lí lớp 11
- SGK Địa lí lớp 11
- Tập bản đồ Lịch sử lớp 11
- SBT Lịch sử lớp 11
- SGK Lịch sử lớp 11