Bài 1. Nguyên tử trang 4, 5 SBT Khoa học tự nhiên 7 Cánh diều
1.1
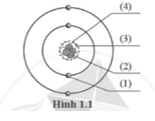
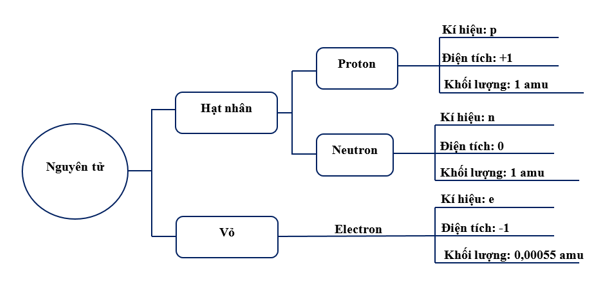
Gọi tên các thành phần của một nguyên tử (hạt nhân, proton, neutron, electron) được mô tả như hình 1.1 dưới đây.
Phương pháp giải:
Lời giải chi tiết:
(1) Electron.
(2) Proton.
(3) Neutron.
(4) Hạt nhân.
1.2
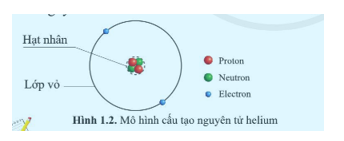
Quan sát hình 1.2, cho biết số proton, neutron, electron và điện tích hạt nhân của mỗi nguyên tử.
Phương pháp giải:
Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.
Lời giải chi tiết:
| Số proton | Số neutron | Số electron |
Boron | 4 | 6 | 4 |
Fluorine | 9 | 10 | 9 |
1.3
Hãy chọn từ cụm từ thích hợp cho sẵn dưới đây để điền vào chỗ ... trong mỗi câu sau: Proton, neutron, electron, hạt nhân nguyên tử, vỏ nguyên tử, nguyên tử.
a) Trong nguyên tử, số proton bằng số .....
b) Hạt nhân nguyên tử gồm ... và ....
c) Phần lớn khối lượng nguyên tử tập trung ở …
d) Trong hạt nhân nguyên tử, hạt ..... không mang điện.
Phương pháp giải:
- Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.
- Khối lượng hạt nhân lớn hơn rất nhiều so với khối lượng vỏ electron nên có thể coi khối lượng nguyên tử tập trung ở hạt nhân.
Lời giải chi tiết:
a) Trong nguyên tử, số proton bằng số electron.
b) Hạt nhân nguyên tử gồm proton và neutron.
c) Phần lớn khối lượng nguyên tử tập trung ở hạt nhân nguyên tử.
d) Trong hạt nhân nguyên tử, hạt neutron không mang điện.
1.4
Mỗi phát biểu sau là đúng hay sai?
a) Các hạt electron được tìm thấy trong hạt nhân của nguyên tử.
b) Các hạt neutron và electron hút nhau.
c) Trong nguyên tử, số electron tối đa ở lớp electron thứ hai là 8.
d) Phần lớn khối lượng của nguyên tử tập trung ở hạt nhân nên kích thước của hạt nhân gần bằng kích thước của nguyên tử.
Phương pháp giải:
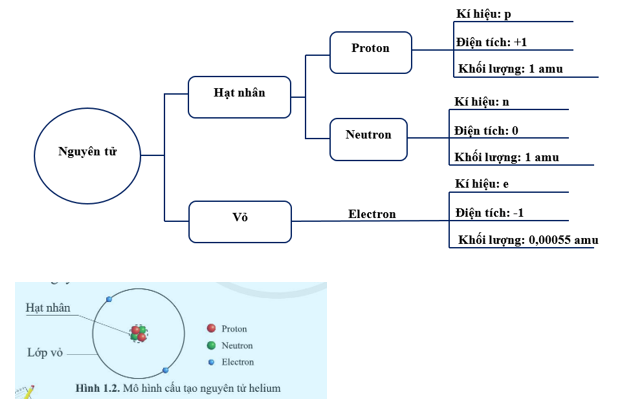
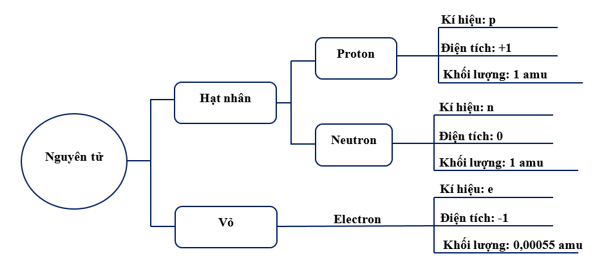
- Nguyên tử gồm hạt nhân và vỏ electron
+ Hạt nhân gồm các hạt proton (mang điện tích dương) và neutron (không mang điện).
+ Vỏ electron gồm các hạt electron (mang điện tích âm).
- Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau:
+ Lớp electron trong cùng (gần hạt nhân nhất) chứa tối đa 2 electron.
+ Lớp electron thứ hai chứa tối đa 8 electron.
- Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.
- Khối lượng hạt nhân lớn hơn rất nhiều so với khối lượng vỏ electron nên có thể coi khối lượng nguyên tử tập trung ở hạt nhân.
Lời giải chi tiết:
- Phát biểu a sai vì các hạt electron nằm ở vỏ nguyên tử.
- Phát biểu b sai vì hạt neutron không mang điện nên electron và neutron không hút nhau.
- Phát biểu c đúng, lớp electron thứ hai trong nguyên tử chứa tối đa 8 electron.
- Phát biểu d đúng, khối lượng hạt nhân lớn hơn rất nhiều so với khối lượng vỏ electron nên có thể coi khối lượng nguyên tử tập trung ở hạt nhân.
1.5
Chọn phát biểu đúng về electron.
A. Một electron có khối lượng lớn hơn một proton và mang điện tích âm.
B. Một electron có khối lượng nhỏ hơn một proton và mang điện tích âm.
C. Một electron có khối lượng nhỏ hơn một neutron và không mang điện tích.
D. Một electron mang điện tích dương và có khối lượng lớn hơn một neutron.
Phương pháp giải:
Lời giải chi tiết:
Electron có khối lượng nhỏ hơn neutron và proton, electron mang điện tích âm.
-> Chọn B.
1.6
Quan sát hình ảnh mô tả cấu tạo nguyên tử nitrogen và silicon (hình 1.3), cho
biết mỗi nguyên tử đó có bao nhiêu lớp electron và số electron trên mỗi lớp electron đó.
Phương pháp giải:
Lời giải chi tiết:
a) Nguyên tử Nitrogen có 2 lớp electron.
+ Lớp thứ nhất có 2 electron.
+ Lớp thứ hai có 5 electron.
b) Nguyên tử Silicon có 3 lớp electron.
+ Lớp thứ nhất có 2 electron.
+ Lớp thứ hai có 8 electron.
+ Lớp thứ ba có 4 electron.
1.7
Cho biết nguyên tử sulfur (lưu huỳnh) có 16 electron. Hãy vẽ sơ đồ mô tả sự phân bố electron trên các lớp electron của nguyên tử sulfur và cho biết mỗi lớp electron có bao nhiêu electron.
Phương pháp giải:
- Nguyên tử gồm hạt nhân và vỏ electron
+ Hạt nhân gồm các hạt proton (mang điện tích dương) và neutron (không mang điện).
+ Vỏ electron gồm các hạt electron (mang điện tích âm).
- Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau:
+ Lớp electron trong cùng (gần hạt nhân nhất) chứa tối đa 2 electron.
+ Lớp electron thứ hai chứa tối đa 8 electron.
- Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.
Lời giải chi tiết:
Nguyên tử sulfur (lưu huỳnh) có 16 electron và 16 proton, nên điện tích hạt nhân của sulfur là 16+
Sơ đồ mô tả sự phân bố electron trên các lớp electron của nguyên tử sulfur
Nguyên tử Sulfur có 3 lớp electron.
+ Lớp thứ nhất có 2 electron.
+ Lớp thứ hai có 8 electron.
+ Lớp thứ ba có 16 – (2+8) = 6 electron.
1.8
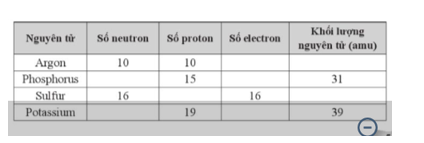
Hoàn thành bảng sau bằng cách điền thông tin thích hợp vào các ô trống:
Phương pháp giải:
- Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.
Số electron = Số proton.
- Khối lượng hạt nhân lớn hơn rất nhiều so với khối lượng vỏ electron nên có thể coi khối lượng nguyên tử tập trung ở hạt nhân.
KLNT (Khối lượng nguyên tử) = số proton x 1 + số neutron x 1 (amu)
-> Số proton = KLNT – số neutron
-> Số neutron = KLNT – số proton
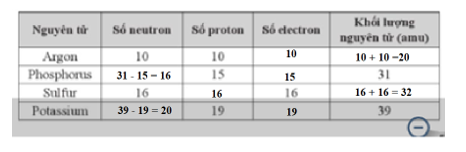
Lời giải chi tiết:
1.9
Tổng số proton, neutron và electron của nguyên tử X là 46. Trong đó, số hạt mang điện nhiều hơn số hạt không mang điện là 14.
a) Tính số proton, số neutron và số electron của nguyên tử X.
b) Tính khối lượng nguyên tử X.
c) Cho biết nguyên tử X có bao nhiêu lớp electron và chỉ ra số electron trên mỗi lớp.
Phương pháp giải:
- Nguyên tử gồm hạt nhân và vỏ electron
+ Hạt nhân gồm các hạt proton (mang điện tích dương) và neutron (không mang điện).
+ Vỏ electron gồm các hạt electron (mang điện tích âm).
- Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau:
+ Lớp electron trong cùng (gần hạt nhân nhất) chứa tối đa 2 electron.
+ Lớp electron thứ hai chứa tối đa 8 electron.
- Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.
- Khối lượng hạt nhân lớn hơn rất nhiều so với khối lượng vỏ electron nên có thể coi khối lượng nguyên tử tập trung ở hạt nhân.
KLNT (Khối lượng nguyên tử) = số proton x 1 + số neutron x 1 (amu)
Lời giải chi tiết:
a) Tổng số proton, neutron và electron của nguyên tử X là 46
p + e + n = 46 (mà p = e)
p + p + n = 46
2p + n = 46
→ n = 46 – 2p
Số hạt mang điện nhiều hơn số hạt không mang điện là 14.
p + e – n = 14 (mà p = e)
p + p – n =14
2p – n = 14
n = 2p – 14
Mặt khác n = 46 – 2p
→ 2p – 14 = 46 – 2p
2p + 2p = 46 + 14
4p = 60
→ p = 60 : 4 = 15
→ e = p = 15
→ n = 2p – 14 = 2.15 – 14 = 16
b) Tính khối lượng nguyên tử X.
KLNT (X) = 15.1 + 16.1 = 31 (amu)
c) Nguyên tử X có 3 lớp electron.
+ Lớp thứ nhất có 2 electron.
+ Lớp thứ hai có 8 electron.
+ Lớp thứ ba có 15 – (2+8) = 5 electron.
1.10
Tổng số proton, neutron và electron của nguyên tử X là 10.
a) Xác định số proton, số neutron và số electron của nguyên tử X. Biết trong nguyên tử X, số neutron lớn hơn số electron và nhỏ hơn 1,5 lần số electron.
b) Xác định số đơn vị điện tích hạt nhân của X.
c) Tính khối lượng nguyên tử X.
d) Cho biết nguyên tử X có bao nhiêu lớp electron và xác định số electron lớp ngoài cùng của X.
Phương pháp giải:
- Nguyên tử gồm hạt nhân và vỏ electron
+ Hạt nhân gồm các hạt proton (mang điện tích dương) và neutron (không mang điện).
+ Vỏ electron gồm các hạt electron (mang điện tích âm).
- Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau:
+ Lớp electron trong cùng (gần hạt nhân nhất) chứa tối đa 2 electron.
+ Lớp electron thứ hai chứa tối đa 8 electron.
- Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.
- Khối lượng hạt nhân lớn hơn rất nhiều so với khối lượng vỏ electron nên có thể coi khối lượng nguyên tử tập trung ở hạt nhân.
KLNT (Khối lượng nguyên tử) = số proton x 1 + số neutron x 1 (amu)
Lời giải chi tiết:
p + e + n = 10 (mà p = e)
e + p + n = 10
2e + n = 10
→ n = 10 – 2e
Số neutron lớn hơn số electron và nhỏ hơn 1,5 lần số electron.
e < n < 1,5e
e < 10 – 2e < 1,5e
e < 10 – 2e và 10 – 2e < 1,5e
e + 2e < 10 và 10 < 1,5e + 2e
3e < 10 và 10 < 3,5e
→ e < 10 : 3 và 10 : 3,5 < e
→e < 3,33 và e > 2,86
Vì số e là số nguyên nên e = 3.
→ p = e = 3.
→ n = 10 – 2e = 10 – 2.3 = 4.
b) Nguyên tử X có 3 proton, nên điện tích hạt nhân của X là 3+
c) Tính khối lượng nguyên tử X.
KLNT (X) = 3.1 + 4.1 = 7 (amu)
d) Nguyên tử X có 2 lớp electron.
+ Lớp thứ nhất có 2 electron.
+ Lớp thứ hai có 3 – 2 = 1 electron.
1.11
Khối lượng của nguyên tử A là 3 amu.
a) Xác định số proton, số neutron và số electron của nguyên tử A, biết trong A, số electron nhỏ hơn số neutron.
b) Cho biết số electron lớp ngoài cùng của A.
Phương pháp giải:
- Nguyên tử gồm hạt nhân và vỏ electron
+ Hạt nhân gồm các hạt proton (mang điện tích dương) và neutron (không mang điện).
+ Vỏ electron gồm các hạt electron (mang điện tích âm).
- Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau:
+ Lớp electron trong cùng (gần hạt nhân nhất) chứa tối đa 2 electron.
+ Lớp electron thứ hai chứa tối đa 8 electron.
- Nguyên tử trung hòa về điện nên tổng số hạt proton bằng tổng số hạt electron.
- Khối lượng hạt nhân lớn hơn rất nhiều so với khối lượng vỏ electron nên có thể coi khối lượng nguyên tử tập trung ở hạt nhân.
KLNT (Khối lượng nguyên tử) = số proton x 1 + số neutron x 1 (amu)
Lời giải chi tiết:
a) Khối lượng của nguyên tử A là 3 amu.
KLNT = số proton x 1 + số neutron x 1
3 = p x 1 + n x 1
→ p + n = 3 (mà p = e)
→ e + n = 3
Trong A, số electron nhỏ hơn số neutron.
e < n → e = 1 và n = 2
→ p = e = 1
b) Nguyên tử A có 1 electron nên A có 1 lớp electron (đây cũng là lớp electron ngoài cùng)
SBT KHTN lớp 7 - Cánh diều
Để học tốt SBT KHTN lớp 7 - Cánh diều, loạt bài giải bài tập SBT KHTN lớp 7 - Cánh diều đầy đủ kiến thức, lý thuyết và bài tập được biên soạn bám sát theo nội dung sách giáo khoa Lớp 7.
- Chủ đề 1. Nguyên tử. Nguyên tố hóa học
- Chủ đề 2. Sơ lược về bảng tuần hoàn các nguyên tố hóa học
- Chủ đề 3. Phân tử
- Chủ đề 8. Trao đổi chất và chuyển hóa năng lượng ở sinh vật
- Chủ đề 9. Cảm ứng ở sinh vật
- Chủ đề 10. Sinh trưởng và phát triển ở sinh vật
- Chủ đề 11. Sinh sản ở sinh vật
- Chủ đề 12. Cơ thể sinh vật là một thể thống nhất
Lớp 7 | Các môn học Lớp 7 | Giải bài tập, đề kiểm tra, đề thi Lớp 7 chọn lọc
Danh sách các môn học Lớp 7 được biên soạn theo sách giáo khoa mới của bộ giáo dục đào tạo. Kèm theo lời giải sách bài tập, sách giáo khoa, đề kiểm tra 15 phút, 45 phút (1 tiết), đề thi học kì 1 và học kì 2 năm học 2025 ngắn gọn, chi tiết dễ hiểu.
Toán Học
- Tài liệu Dạy - học Toán 7
- Sách bài tập Toán 7 - Cánh diều
- Sách bài tập Toán 7 - Chân trời sáng tạo
- Sách bài tập Toán 7 - Kết nối tri thức
- SGK Toán 7 - Cánh diều
- SGK Toán 7 - Chân trời sáng tạo
- SGK Toán 7 - Kết nối tri thức
Ngữ Văn
- SBT Ngữ văn lớp 7
- Văn mẫu 7 - Cánh Diều
- Văn mẫu 7 - Chân trời sáng tạo
- Văn mẫu 7 - Kết nối tri thức
- SBT Văn 7 - Cánh diều
- SBT Văn 7 - Chân trời sáng tạo
- SBT Văn 7 - Kết nối tri thức
- Tác giả - Tác phẩm văn 7
- Soạn văn 7 - Cánh diều chi tiết
- Soạn văn 7 - Cánh diều siêu ngắn
- Soạn văn 7 - Chân trời sáng tạo chi tiết
- Soạn văn 7 - Chân trời sáng tạo siêu ngắn
- Soạn văn 7 - Kết nối tri thức chi tiết
- Soạn văn 7 - Kết nối tri thức siêu ngắn
GDCD
Tin Học
- SBT Tin học 7 - Kết nối tri thức
- SGK Tin học 7 - Cánh Diều
- SGK Tin học 7 - Chân trời sáng tạo
- SGK Tin học 7 - Kết nối tri thức
Tiếng Anh
- SBT Tiếng Anh lớp 7
- SBT Tiếng Anh 7 - English Discovery
- SBT Tiếng Anh 7 - Right on!
- SBT Tiếng Anh 7 - iLearn Smart World
- SBT Tiếng Anh 7 - Friends Plus (Chân trời sáng tạo)
- SBT Tiếng Anh 7 - Global Success (Kết nối tri thức)
- Tiếng Anh 7 - English Discovery
- Tiếng Anh 7 - Right on!
- Tiếng Anh 7 - iLearn Smart World
- Tiếng Anh 7 - Friends Plus
- Tiếng Anh 7 - Global Success
Công Nghệ
- SGK Giáo dục công dân 7 - Cánh diều
- SGK Giáo dục công dân 7 - Chân trời sáng tạo
- SGK Giáo dục công dân 7 - Kết nối tri thức
- SGK Công nghệ 7 - Cánh diều
- SGK Công nghệ 7 - Chân trời sáng tạo
- SGK Công nghệ 7 - Kết nối tri thức
Khoa Học Tự Nhiên
- SBT KHTN lớp 7 - Cánh diều
- SBT KHTN lớp 7 - Chân trời sáng tạo
- SBT KHTN lớp 7 - Kết nối tri thức
- SGK Khoa học tự nhiên 7 - Cánh diều
- SGK Khoa học tự nhiên 7 - Chân trời sáng tạo
- SGK Khoa học tự nhiên 7 - Kết nối tri thức
Lịch Sử & Địa Lý
- SBT Lịch sử và Địa lí 7 - Chân trời sáng tạo
- SBT Lịch sử và Địa lí 7 - Kết nối tri thức
- SGK Lịch sử và Địa lí lớp 7 - Cánh Diều
- SGK Lịch sử và Địa lí lớp 7 - Chân trời sáng tạo
- SGK Lịch sử và Địa lí lớp 7 - Kết nối tri thức