Bài 1 trang 60 SGK Hóa học 8
Đề bài
Hình dưới đây là sơ đồ tượng trưng cho phản ứng giữa khí N2 và khí H2 tạo ra amoniac NH3 :
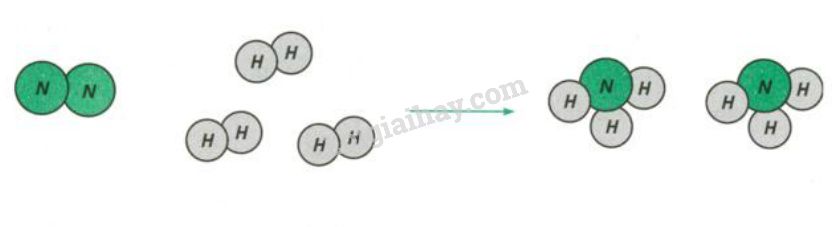
Hãy cho biết :
a) Tên các chất tham gia và sản phẩm của phản ứng.
b) Liên kết giữa các nguyên tử thay đổi như thế nào ? Phân tử nào biến đổi, phân tử nào được tạo ra ?
c) Số nguyên tử mỗi nguyên tố trước và sau phản ứng bằng bao nhiêu, có giữ nguyên không ?
Chú thích
Về điều kiện cho phản ứng xảy ra hãy xem trong bài đọc thêm sau bài 13, trang 51. Để nhận biết có chất mới là amoniac ta thử một tính chất của amoniac mà các em đã có dịp biết trong thí nghiệm 1, bài 7. Bài thực hành 2, trang 28.
Lời giải chi tiết
a) Chất tham gia: nitơ N2, hiđro H2
Sản phẩm: amoniac NH3
b) Trước phản ứng, hai nguyên tử hiđro liên kết với nhau, hai nguyên tử nitơ cũng vậy. Sau phản ứng, ba nguyên tử hiđro liên kết với một nguyên tử nitơ. Phân tử hiđro và phân tử nitơ biến đổi, phân tử amoniac được tạo ra.
c) Số nguyên tử nguyên tố N trước và sau phản ứng đều là 2. Số nguyên tử nguyên tố H trước và sau phản ứng đều bằng 6.
Như vậy, số nguyên tử mỗi nguyên tố trước và sau phản ứng không thay đổi.
Xemloigiai.com
- Bài 2 trang 60 SGK Hóa học 8
- Bài 3 trang 61 SGK Hóa học 8
- Bài 4 trang 61 SGK Hóa học 8
- Bài 5 trang 61 SGK Hóa học 8
SGK Hóa lớp 8
Giải bài tập hóa học lớp 8 đầy đủ công thức, lý thuyết, phương trình hóa học, chuyên đề hóa học SGK 8 giúp để học tốt hóa học 8
MỞ ĐẦU
CHƯƠNG 1: CHẤT - NGUYÊN TỬ - PHÂN TỬ
- Bài 2. Chất
- Bài 3. Bài thực hành 1
- Bài 4. Nguyên tử
- Bài 5. Nguyên tố hóa học
- Bài 6. Đơn chất và hợp chất - Phân tử
- Bài 7. Bài thực hành 2
- Bài 8. Bài luyện tập 1
- Bài 9. Công thức hóa học
- Bài 10. Hóa trị
- Bài 11. Bài luyện tập 2
- Đề kiểm tra 15 phút - Chương 1 - Hóa học 8
- Đề kiểm tra 45 phút (1 tiết) - Chương 1 - Hóa học 8
Đề kiểm tra giữa học kì - Hóa học 8
CHƯƠNG 2: PHẢN ỨNG HÓA HỌC
- Bài 12. Sự biến đổi chất
- Bài 13. Phản ứng hóa học
- Bài 14. Bài thực hành 3
- Bài 15. Định luật bảo toàn khối lượng
- Bài 16. Phương trình hóa học
- Bài 17. Bài luyện tập 3
- Đề kiểm tra 15 phút - Chương 2 - Hóa học 8
- Đề kiểm tra 45 phút (1 tiết) - Chương 2 - Hóa học 8
CHƯƠNG 3: MOL VÀ TÍNH TOÁN HÓA HỌC
- Bài 18. Mol
- Bài 19. Chuyển đổi giữa khối lượng thể tích và lượng chất
- Bài 20. Tỉ khối của chất khí
- Bài 21. Tính theo công thức hóa học
- Bài 22. Tính theo phương trình hóa học
- Bài 23. Bài luyện tập 4
- Đề kiểm tra 15 phút - Chương 3 - Hóa học 8
- Đề kiểm tra 45 phút (1 tiết) - Chương 3 - Hóa học 8
Đề thi học kì 1 mới nhất có lời giải
CHƯƠNG 4: OXI - KHÔNG KHÍ
- Bài 24. Tính chất của oxi
- Bài 25. Sự oxi hóa – Phản ứng hóa hợp - Ứng dụng của oxi
- Bài 26. Oxit
- Bài 27. Điều chế khí oxi - Phản ứng phân hủy
- Bài 28. Không khí - Sự cháy
- Bài 29. Bài luyện tập 5
- Bài 30. Bài thực hành 4
- Đề kiểm tra 15 phút - Chương 4 - Hóa học 8
- Đề kiểm tra 45 phút (1 tiết) - Chương 4 - Hóa học 8
CHƯƠNG 5: HIĐRO - NƯỚC
- Bài 31. Tính chất - Ứng dụng của hiđro
- Bài 32. Phản ứng oxi hóa - khử
- Bài 33. Điều chế khí hiđro - Phản ứng thế
- Bài 34. Bài luyện tập 6
- Bài 35. Bài thực hành 5
- Bài 36. Nước
- Bài 37. Axit - Bazơ - Muối
- Bài 38. Bài luyện tập 7
- Bài 39. Bài thực hành 6
- Đề kiểm tra 15 phút - Chương 5 - Hóa học 8
- Đề kiểm tra 45 phút (1 tiết) - Chương 5 - Hóa học 8
CHƯƠNG 6: DUNG DỊCH
- Bài 40. Dung dịch
- Bài 41. Độ tan của một chất trong nước
- Bài 42. Nồng độ dung dịch
- Bài 43. Pha chế dung dịch
- Bài 44. Bài luyện tập 8
- Bài 45. Bài thực hành 7
- Đề kiểm tra 15 phút - Chương 6 - Hóa học 8
- Đề kiểm tra 45 phút (1 tiết) - Chương 6 - Hóa học 8
ĐỀ KIỂM TRA HỌC KÌ 2 (ĐỀ THI HỌC KÌ 2) - HÓA HỌC 8
Xem Thêm
Lớp 8 | Các môn học Lớp 8 | Giải bài tập, đề kiểm tra, đề thi Lớp 8 chọn lọc
Danh sách các môn học Lớp 8 được biên soạn theo sách giáo khoa mới của bộ giáo dục đào tạo. Kèm theo lời giải sách bài tập, sách giáo khoa, đề kiểm tra 15 phút, 45 phút (1 tiết), đề thi học kì 1 và học kì 2 năm học 2025 ngắn gọn, chi tiết dễ hiểu.
Toán Học
Vật Lý
Hóa Học
Ngữ Văn
- SBT Ngữ văn lớp 8
- Tác giả - Tác phẩm văn 8
- Văn mẫu lớp 8
- Vở bài tập Ngữ văn lớp 8
- Soạn văn 8 chi tiết
- Soạn văn 8 ngắn gọn
- Soạn văn 8 siêu ngắn
Sinh Học
GDCD
Tin Học
Tiếng Anh
Công Nghệ
Lịch Sử & Địa Lý
- SBT Lịch sử lớp 8
- Tập bản đồ Địa lí lớp 8
- SBT Địa lí lớp 8
- VBT Địa lí lớp 8
- SGK Địa lí lớp 8
- Tập bản đồ Lịch sử lớp 8
- SBT Lịch sử lớp 8
- VBT Lịch sử lớp 8
- SGK Lịch sử lớp 8